胃がん
l. 胃癌とは
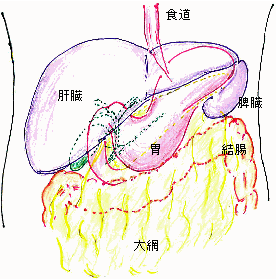
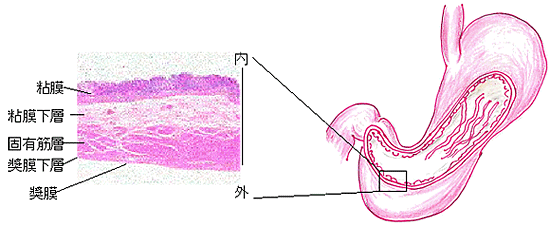
胃は上腹部に位置し、入口は食道、出口は十二指腸とつながっている袋状の臓器です。胃の主な働きは口から入った食物を一時的にたくわえ、胃液と混ぜ合わせこなした後に、少量ずつ十二指腸に送ることです。胃液は強い酸と消化酵素により消化を助け、また口から入った細菌を殺菌します。胃の壁は内側から粘膜、粘膜下層、筋肉層および漿膜からなります。その周囲には胃を栄養する種々の血管と、免疫をつかさどる組織であるリンパ節が多数存在します。癌の進行度は胃壁への深達度、腹腔内への癌細胞の播種の有無、リンパ節への転移の有無・程度、そして他臓器への転移の有無によって決定されます。
また、胃の壁から分泌される内因子は血液(赤血球)を作るのに必要なビタミンB12の吸収に関与しており、胃切除後(全摘)には巨赤芽球性貧血を生じることがあります。
"がん"は遺伝子の異常により発症する病気です。"がん"のうち上皮細胞から発生するのが狭義の"癌"で、それ以外の固形組織から発生するものを "肉腫" と言います。胃癌は胃の上皮(粘膜細胞)から発生します。癌細胞の遺伝子異常は一つだけでなく、いくつかの重要な遺伝子が様々な傷(変異)を生じ発生すると言われています。発生してからは10数年かけて診断可能な大きさ(5mm以上)になるとされています。慢性胃炎、食生活、ヘリコバクター・ピロリ(細菌)などが胃がんの発生に関与すると言われています。2005年には、ヘリコバクター・ピロリの発見者MarshallとWarrenがノーベル医学生理学賞を受賞しています。
ll. 症状
胃癌に伴う症状は、初期の段階では特定なものはありません。腫瘍が大きくなると、出血、通過障害を生じてきます。また、出血に伴う貧血症状で発見されることもあります。スキルス癌のように浸潤性の強い癌では、発見時にはすでに切除ができない病状まで進んでしまっていることもあります。
lll. 診断
癌の診断方法は、血液検査、レントゲン検査、内視鏡検査などに分けられます。胃癌では、バリウムを飲んでレントゲン検査を行なう胃透視と上部消化管内視鏡検査の2つが主体です。確定診断には内視鏡下に腫瘍の組織をつまみ(生検)、顕微鏡検査で診断をつけます(病理生検組織診断)。
早期の病変を発見するには内視鏡検査が優れておりますが、検査にはある程度の苦痛を伴い、合併症の可能性もあります。現在、集団検診ではペプシノーゲン法と胃バリウムレントゲン透視が主に行われており、それで要精査となった人が内視鏡検査を受けるシステムが多いようです。ペプシノーゲン法は、癌そのものを探り当てるのではなく、高分化腺癌との関連があると言われている慢性胃炎の患者さんを拾い上げ、内視鏡検査で癌を発見する方法です。
さて、癌と診断された場合には治療方針を決定するために、その進行度を調べなければなりません。進行度は、下記のように胃壁への深達程度、リンパ節、他臓器への転移、腹膜転移(播種)で決定されます。これらの診断にはCT。MRI、超音波検査等が主に行われますが、その他にも種々の検査を組み合わせ進行度を決めることもあります。
血液検査の腫瘍マーカーは、治療効果の判定、再発診断に主に利用されています。 "腫瘍マーカーで癌の早期診断が出来ないのか?"という質問をよく受けますが、現時点では早期胃癌を発見できる血液の腫瘍マーカーはありません。
lV. 病期
癌の病期(進行度、stage)は、前述したように胃壁への深達程度、リンパ節、他臓器への転移、腹膜転移(播種)で決定されます。本邦では粘膜下層までの胃癌を早期胃癌、筋肉層より深く進展(浸潤)したものを進行胃癌と大きく分類しています。本邦としたのは、日本の胃癌学会と国際的なUICCとでは進行度の分類が、若干異なるからです。胃癌に関しては日本は欧米に比較して発症率が高く、手術で系統的なリンパ節郭清が行われることが多く、なおかつ合併症が低く手術成績が良好であることなど、胃癌治療の先進国を自負しています。従って、病期分類も国際的な基準より細かく設定されています。
次に、日本胃癌学会の胃癌病期分類を示します。

転移/浸潤とは・・・
胃癌の転移には、リンパ管を介するリンパ節転移、血液を介する肝転移などの遠隔臓器転移、癌が胃壁の表面(漿膜)まで浸潤し、そこからこぼれ落ち腹膜に生着する腹膜播種(転移)が主なものです。初期にはリンパ節転移が最も多く、進行するにつれ肝転移などの血行性転移、腹膜転移がおこります。
リンパ節転移もある段階までは局所の病変として手術による治癒切除が可能ですが、高度な転移は全身的な病気の広がりの目印と考えられます。腹膜播種は、小腸、大腸、膀胱などの臓器に付着し、腹水を生じたり腸を狭くする原因となります。
V. 治療
早期癌が約半数を占めるようになり、そのうち半数弱の方にはより負担の少ない内視鏡治療が選択されるようになってきました。進行胃癌の治療法は主に外科的な切除で、また転移や浸潤が高度な場合は内科的な治療(抗癌剤等)が中心となります。胃癌学会では日常診療と研究的な治療に分けた胃がん治療ガイドライン(2001年、金原出版)を発表しましたのでご参照ください。以下に具体的な適応と方法を解説します。
(1)内視鏡治療
胃癌学会のガイドラインでは2cm以下の分化型(限局したタイプ)の粘膜内がんに対して内視鏡による粘膜切除(EMR)を標準的治療としています。最近では粘膜内に限局している病変に対しては、2cmを超えていても広範囲に粘膜切除が可能な粘膜切開・剥離法(ESD)で治療している施設もあります。また、高齢や合併する病変で手術が不可能な患者さんに対しては、ガイドライン適応外の病変にも内視鏡治療を行う場合もあります。
EMRやESDによる偶発症(出血や穿孔)は、内視鏡的な止血や縫縮(穴をふさぐ)で対処できることが多いのですが、手術で対処しなければならない場合もあります。また、切除された標本の顕微鏡検査で粘膜下層への浸潤、または静脈やリンパ管内に癌が認められた時、再発を認められた時には追加の手術が必要な場合があります。また早期癌の10-20%は多発するため、定期的な内視鏡検査が必要です。
(2)手術治療
手術による切除はがんを局所的にコントロールする最も効果的な手段です。外科手術は、癌が肉眼的にとりきれる場合(根治手術)と、癌による症状出現の予防や出血や狭窄を改善するための姑息的手術(緩和的手術)とに分けられます。
胃の切除範囲は癌の発生部位と進展度で決定され、食道側(入口側)では噴門側胃切除や胃全摘、十二指腸側(出口側)では幽門側胃切除(下2/3切除)が行われます。日本におけるリンパ節郭清(切除)は進行胃癌では第2群(胃癌治療ガイドラインを参照)までの切除が標準ですが、早期癌では切除範囲を縮小する場合が多く、小さな傷で体に対する侵襲を低減させうる、腹腔鏡補助手術も行なわれております。腹腔鏡補助下の手術適応は施設により異なる場合が多く、当院では粘膜下層(sm)までの浸潤で、明らかなリンパ節転移のない症例を対象としております。また、早期癌で胃の中央部に病変が存在する場合には、分節胃切除や幽門輪温存幽門側胃切除術といった胃の中央部だけを切除する術式が選択される場合もあります。逆に、癌が周囲組織に浸潤している場合には膵臓、横行結腸、左副腎などを合併切除する場合もあります。
胃を切除された後では、胃の貯留能や食物をこなす能力が損なわれます。それを補うためには、口で十分時間をかけ食物をよく噛むことが必要です。手術後には栄養士による食事指導を行なっておりますので、ご活用下さい。
次に代表的な胃癌の手術術式について説明します。
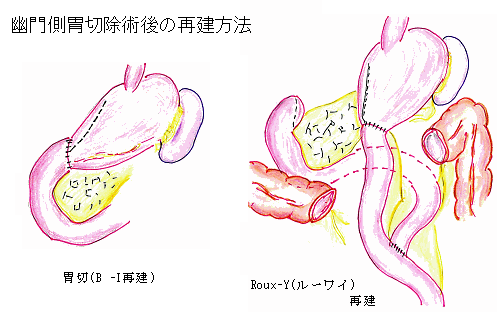
<幽門側胃切除>
切除後の再建には、残胃と十二指腸とをつなぐ方法(Billroth-Ⅰ法)と残胃と空腸とをつなぐ方法(Billroth-Ⅱ法、Roux-en Y)とがあります。通常はBillroth-Ⅰ法で再建することが多く、残胃が小さく吻合に緊張が生じる場合、食道裂孔ヘルニアなどで術後逆流性食道炎が生じる可能性が高い場合にはBillroth-Ⅱ法あるいはRoux-en Yで再建するようにしています。
これまでは、十二指腸を食物が通過することを重要視し、Billroth-Ⅰ法での再建が主体でした。しかし、最近は残胃への胆汁逆流に伴う残胃炎や逆流性食道炎の予防のため、Roux-en Yでの再建を積極的に行う施設もみられます。
また、リンパ節郭清をしっかり行なった場合には、胆嚢に分布する神経が途切れてしまい、胆嚢の収縮が十分できなくなり、胆嚢結石症や胆嚢炎を合併しやすくなるため、あらかじめ胃の手術時に胆嚢を併せて切除する場合もあります。
<胃全摘術>
胃の全体を切除する手術です。リンパ節を2群まで切除する場合には、脾臓を併せて切除する場合もあります。胃を切除した後には、食道と十二指腸は直接つなぐことはできないので、十二指腸の切離端は閉鎖し、空腸を一旦切離、食道と空腸をつなぎ合わせ、さらに空腸同士をつないで再建しています(Roux- en Y)。
その他には、挙上し空腸を折り曲げ空腸同士を吻合し大きな袋状にし食物の貯留能を期待する方法(空腸Pouch吻合)や、十二指腸と食道の間に胃の代わりに空腸を置換する方法(空腸interposition)などいくつかの再建方法が考案されていますが一般的ではなく、当院ではRoux-en Y再建を行なっています。
また、幽門側胃切除術と同様にリンパ節郭清をしっかり行なった場合、胆嚢を併せて切除する場合もあります。
胃全摘術後の再建方法
Roux-Y(ルーワイ)再建
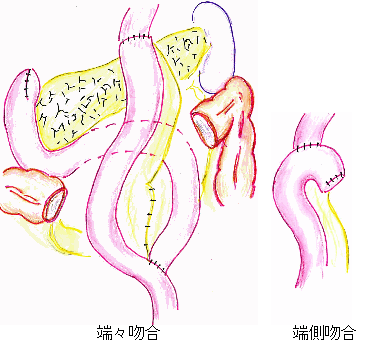
<バイパス術>
癌が周囲臓器に浸潤し切除できない場合、切除するメリットよりもデメリットが大きい場合には胃を切除することなく、食事摂取が可能となることを目的として胃と小腸とをつないでバイパスをつくる手術を行なう場合があります。食物の通過障害がなくても、食事をとることにより消化管出血がみられる場合にも、出血予防のためバイパス術の適応となることがあります。バイパス術には下図のように胃をパーテーションで区切るようにし、口側の癌のない部分と小腸とをつなげる手術を第1としますが、癌の進展が高度で区切りを作る余裕のない場合には、癌の浸潤がない部分で胃と空腸とをつなぐ場合もあります。
また、バイパス術もおけない場合には、栄養摂取を目的として腸瘻のみを造設する場合もあります。
非切除症例でのバイパス術
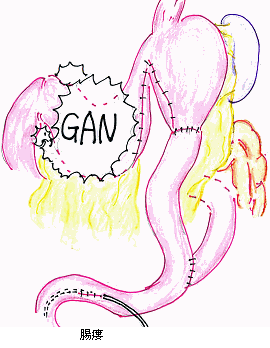
(3)補助療法
癌の進行が高度で切除ができない場合、また転移や浸潤が高度な場合は化学療法(抗癌剤治療)を行ないます。現在、胃癌対する化学療法はTS-1という内服薬が主体です。癌の進行度、再発の有無などを考慮し化学療法の内容を提示し、最終的には患者さんと相談のうえ治療内容を決定します。
以下に、当院での大まかな指針を示します。
stagelA, lB
化学療法の適応としない。
stagell
化学療法の適応とする。経口5FU製剤の内服を基本とする。
病理組織診断で再発の可能性が高いと思われる場合にはTS-1を選択
stage lllA、lllB
基本的に化学療法の適応とする。TS-1の内服を基本とする。
stagelV および遺残・再発癌
化学療法の絶対適応
1st line TS-1( + CDDP)
2nd line以降は状況に応じて決定する
# stagelV および遺残・再発癌では一つのレジメン(治療方法)にこだわることなく、使用できる抗癌剤はすべて使うつもりで治療を行っていく。
VI. 治療成績
当院外科における、胃癌術後治療成績を示します。胃癌学会の治療ガイドラインに沿った治療を行っており、治療成績も全国統計とほぼ同様な傾向を示しております。